胶原蛋白类填充剂的临床前研究服务―赫贝科技
人体皮肤中真皮的构成70%是胶原蛋白,主要的功能是维持皮肤和皮肤的弹性。脸部胶原蛋白的填充,主要是用于填充深的皱纹,皮肤损伤所致的缺损和修补脸型缺陷。为了修补皮肤的某处缺陷,求美者通过填充剂或者其他药物达到理想的效果。
胶原蛋白类填充剂作为第1代填充类产品,牛胶原蛋白作为软组织填充的历史可追溯至1980年代初期。截至目前,国内已获批上市的胶原蛋白"填充类"产品有:双美旗下的“肤柔美”、“肤丽美”和“肤力原”,博泰旗下的“弗缦”(原名“肤美达”),荷兰汉福旗下“爱贝芙”,锦波生物旗下的“薇旖美”。
在医疗美容领域,目前境内已批准的填充剂(注射)产品名称包括:重组Ⅲ型人源化胶原蛋白冻干纤维、胶原蛋白植入剂、含利多卡因胶原蛋白植入剂、医用胶原充填剂等。其中,重组Ⅲ型人源化胶原蛋白冻干纤维是目前为止国家药监局第一个发文并认可的,我国自主研制的采用新型生物材料――重组人源化胶原蛋白制备的三类医疗器械产品。
2022年12月29日,国家药监局器审中心对外发布整形美容用重组人源化胶原蛋白注射材料技术审评要点(试行)等3项技术审评要点,其中整形美容用重组人源化胶原蛋白注射材料技术审评要点针对产品注册申报前的可能需要进行的动物实验指出,动物试验研究应参照《医疗器械动物试验研究注册审查指导原则 第一部分:决策原则》确定是否需要进行动物试验。对于经决策需开展动物试验的,参照《医疗器械动物试验研究注册审查指导原则 第二部分:试验设计、实施质量保证》设计并开展动物试验,提供规范的相应研究目的的动物试验研究资料,如动物体内降解代谢的研究资料等。在准备用于证明产品安全有效性的研究资料时,对于以医疗器械作用为主的添加药品成分的整形美容用重组人源化胶原蛋白注射材料类产品,需按照药械组合产品的相关法规及《以医疗器械作用为主的药械组合产品注册审查指导原则》、《以医疗器械作用为主的药械组合产品中药物定性定量及体外释放研究注册审查指导原则》提供相应资料。
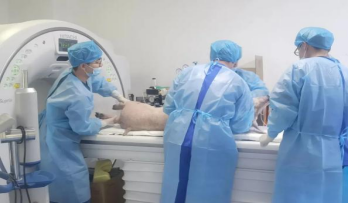
杭州赫贝科技有限公司(以下简称赫贝)提供符合CNAS规范的综合性临床前研究服务,与多个企业合作,开发了胶原蛋白类填充剂的非临床动物实验体内验证方法,提供产品炎症反应、胶原增生、产品降解情况等多种风险评估以充分评估产品的安全有效性。针对胶原蛋白类填充剂产品,赫贝在实验方案设计以及执行过程中对动物数量、注射位点、对照品的选择、随访周期等要求严格遵守非临床动物试验设计要求。胶原蛋白填充剂试验部分附图如下。
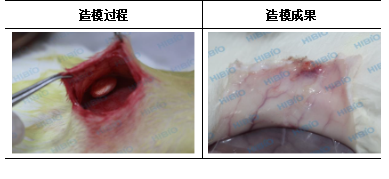
造模图
病理结果图
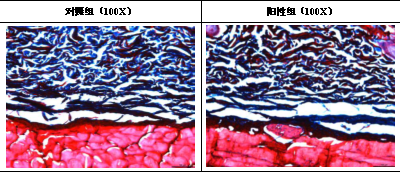
在结果评估上,通过检测动物不同时间节点病理学结果以评估植入后的局部不良反应,同时对产品降解情况进行分析,为面部填充产品研发阶段提供可靠的数据支持。
如需更多资料,请电话咨询:0571-28313118。
公司介绍
医美时代向前,赫贝技术焕新,将持续通过高效率、高质量、高性价比的临床前研究服务,为客户提供更全面的安全有效性评价。
赫贝致力于新药、新医疗器械临床前CRO服务,拥有6000多平方的专业生物实验室和SPF实验动物中心,具备药理毒理评价资质及CNAS实验室质量认可,是浙江省内规模靠前、技术领先的专业临床前CRO企业。
赫贝始终关注创新型医疗器械研发的最新动向以及临床前生物相容性、有效性评价政策法规,已开展多项医疗器械可行性研究和临床前研究项目,推动过多项医疗器械产品通过NMPA审批进入临床阶段和成功上市。旨在加快创新医疗器械产品成果转化,促进医疗卫生事业与大健康产业快速发展。




