2×SYBR Green qPCR试剂(预混ROX1型)
产品名称:2×SYBR Green qPCR试剂(预混ROX1型)
英文名称:2×SYBR Green qPCR Master Mix (ROX1)
货号规格:UR32071(500 Rxns×20μL)
运输存储:冰袋运输,-20℃避光存储。
产品描述:
本试剂盒采用具有超强扩增能力和抗干扰能力的热启动DNA聚合酶,结合其高度优化的缓冲液体系和染料系统,使之具备更强的扩增效率、抗干扰能力,更高的灵敏度和特异性。在相同的情况下具有起峰更早、得到的荧光信号更强、Ct值更小及熔解曲线特异性更高等特点。此外,为了进一步简化操作,本试剂盒的2×SYBR Green qPCR Master Mix预混了ROX1染料(high ROX),从而只需要将模板cDNA、引物以及ddH2O添加进去,即可进行qPCR反应。
产品组分:
组分:2×SYBR Green
规格:qPCR Master Mix(ROX1)* 5 mL
*包含热启动DNA聚合酶, dNTPs, Mg2+, buffer, 和 SYBR Green I染料,且预混了高浓度
ROX(ROX1)用于校正不同孔之间的荧光信号误差。
适用的仪器型号:

(如果仪器不在下表中,请选用UR32081:2×SYBR Green qPCR试剂(预混ROX2型))
产品使用:
1、 使用前,将2×SYBR Green qPCR Master Mix(ROX1)试剂从-20℃冰箱中取出,室温放置5 ~ 10分钟或用手紧握试剂管使之充分融化,上下颠倒5 ~ 10次充分混匀(非常重要),然后使用离心机短暂离心至管底,放在冰上备用。
2、逆转录反应得到的cDNA建议稀释并充分混匀后再作为模板使用,这样可以提高实验的重复性。通常建议稀释5 ~ 10倍后再使用(具体的稀释倍数根据基因表达丰度来确定)。在20 μL的qPCR反应体系中:如果模板cDNA稀释5倍,建议使用2 μL的cDNA(1 ~ 4 μL);如果模板cDNA稀释10倍,建议使用4 μL的cDNA(2 ~ 8 μL);如果模板cDNA稀释20倍,建议使用9.2 μL的cDNA;如果模板cDNA不稀释,建议使用0.4 μL的cDNA(0.2 ~ 0.8 μL)。假定模板cDNA在使用前已经用灭过菌的ddH2O稀释了5倍(20 μL cDNA加80 μL ddH2O稀释至100 μL),按照如下表格进行qPCR反应体系的配制:
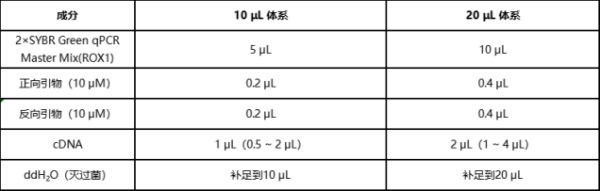
3、qPCR加样体系的配制:为了使加样误差降低到最低,一般建议将cDNA和ddH2O配制成预混液,2×SYBR Green qPCR Master Mix和引物对配制成预混液,分别混匀后再依次加入到每个反应孔中(例如,对于20 μL的qPCR反应体系:每个反应孔中,cDNA和ddH2O的预混液加9.2 μL,2×SYBR GreenqPCR Master Mix和引物对的预混液加10.8 μL);或者根据个人熟练掌握的加样方式进行加样。
4、加样完成后,盖上封板膜并封紧,然后用离心机1000 rpm离心1分钟,将液体离心至qPCR孔板底部。
5、qPCR反应程序如下:
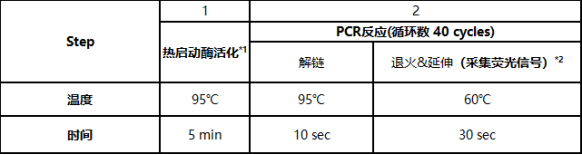
上述反应程序设置好后,按照仪器默认的程序添加熔解曲线。
注意: *1:95℃反应5分钟的目的是活化热启动酶,该步骤为必须步骤,因此不能省略;
*2:在退火&延伸这一步骤需要进行荧光信号的采集。下方表格提供了一种代表性的熔解曲线程序供参考:
Step 1 2 3
加热或降温速度 100% 100% 1%
温度 95℃ 60℃ 95℃
时间 15 sec 1 min 30 sec
采集数据 - - 升温阶段采集荧光信号
关于qPCR反应是否良好的判断:
1、 如果扩增曲线呈典型的S型曲线,荧光背景信号阶段、荧光信号指数扩增阶段及平台期均完整可见,熔解曲线单峰,内参Ct值在合理范围内(通常可在13 ~ 22之间,典型的内参Ct值在15 ~ 20之间),则可认为该反应正常;
2、 同一个模板和引物的重复孔数据Ct值相差0.5以内;
3、 同时满足以上两个条件的可以认为数据可用。
qPCR引物的设计:
1、 通过Google Scholar查询文献当中的引物,通常中等及以上水平期刊中的qPCR引物绝大多数可以直接使用;
2、 NCBI数据库的Blast数据库中的Primer Blast提供了针对序列或者Gene ID的qPCR引物设计方案,每个基因建议设计2对引物进行合成、验证;
3、 Primer Bank数据库中有部分已经验证过的引物可作为参考或者直接合成使用。
常见的注意事项、操作要点及优化方法:
1、 实验开始前首先验证引物是否适用,标准与上述标准类似,主要观察扩增曲线与熔解曲线;
2、 引物验证好用后应分装几份并放在-20℃保存,以防止污染或降解;
3、 RNA及cDNA的质量均对qPCR的结果具有很大的影响,因此应尽量保证RNA不降解。 RNA提取后应尽快进行逆转录,且避免反复冻融。如果预计使用量较大,则可以一次多逆转录几管cDNA。如果不立即使用cDNA,则建议保存在-80℃冰箱。